Coenzyme Q - cytochrome c-réductase
Le complexe cœnzyme Q – cytochrome-c-réductase, ou complexe bc1, est le 3e complexe de la chaîne oxydative mitochondriale, c'est-à-dire de la chaîne de transport des électrons.
Le complexe cœnzyme Q – cytochrome-c-réductase, ou complexe bc1, est le 3e complexe de la chaîne oxydative mitochondriale (complexe III), c'est-à-dire de la chaîne de transport des électrons.
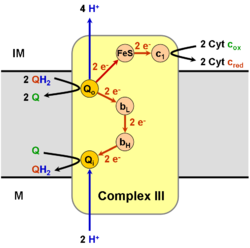
Dans ce complexe, la cytochrome-c-réductase est une enzyme transmembranaire qui catalyse la réduction du cytochrome c, processus au cours duquel 2 ions H+ sont retirés au cœnzyme Q (qui est par conséquent oxydé), ces 2 ions H+ passant dans l'espace inter-membranaire de la mitochondrie (cycle Q). Cela participe à la création d'un gradient osmotique de protons (ions H+) utilisé par l'ATP-synthase (ATP-synthétase) pour la synthèse d'ATP. Deux autres ions H+ sont extraits de la matrice de la mitochondrie reduisant le cœnzyme Q10 pour la réaction suivante.
Le cœnzyme Q, toujours nommé ubiquinone à cause de son caractère ubiquitaire dans les cellules, est un dérivé de benzoquinone, caractérisé par une longue chaîne isoprénoïque (poly-isoprène), qui le rend particulièrement liposoluble, par conséquent capable de l'insérer dans les membranes biologiques. Cette molécule a subi au cours de l'évolution un allongement progressif de la chaîne isoprénoïque (2 unités isoprénoïde chez la bactérie, 6 à 6 chez les animaux, 10 chez l'Homme, d'où son autre nom : CoQ10). Le terme de cœnzyme Q est fréquemment appliqué à la totalité du complexe III de la chaîne oxydative, qui comporte, hormis l'ubiquinone, le cytochrome c1 [qui contient 1 hème]) et le cytochrome b [qui contient 2 hèmes, bL et bH) ])
Le rôle de la chaîne oxydative mitochondriale est de coupler la réduction de l'oxygène moléculaire à la production d'énergie chimique (ATP) utilisable par l'organisme pour ses réactions de biosynthèse. C'est le processus de phosphorylation oxydative. Dans cette chaîne, les électrons libres (provenant de la dégradation des sucres, plus exactement du cycle tricarboxylique) passent de molécule à molécule (flavoprotéines, cytochromes, enzymes membranaires mitochondriales) au sein de complexes multimoléculaires, chaque passage permettant d'«amortir» le saut d'énergie. Dans cette chaîne, le cœnzyme Q (complexe III) accepte les électrons provenant des complexes I et II, pour les faire passer au complexe IV (qui couple l'oxydation du cytochrome c à la réduction de l'oxygène en eau). L'oxygène, accepteur final des électrons, est par conséquent, en fin de compte, réduit par formation d'une molécule d'eau pour chaque paire d'électrons transportée. Au passage est créé, entre les différents compartiments de la mitochondrie, un gradient d'ions H+ utilisé pour la synthèse de l'ATP par l'ATP-synthase (qui est par conséquent nommée complexe V).
Liens externes
Recherche sur Google Images : |
|
"Coenzyme Q-10 + Lécithine" L'image ci-contre est extraite du site pharmaciesainthelier.fr Il est possible que cette image soit réduite par rapport à l'originale. Elle est peut-être protégée par des droits d'auteur. Voir l'image en taille réelle (308 x 371 - 17 ko - jpg)Refaire la recherche sur Google Images |
Recherche sur Amazone (livres) : |
Voir la liste des contributeurs.
La version présentée ici à été extraite depuis cette source le 06/11/2009.
Ce texte est disponible sous les termes de la licence de documentation libre GNU (GFDL).
La liste des définitions proposées en tête de page est une sélection parmi les résultats obtenus à l'aide de la commande "define:" de Google.
Cette page fait partie du projet Wikibis.


 Accueil
Accueil Recherche
Recherche Début page
Début page Contact
Contact Imprimer
Imprimer Accessibilité
Accessibilité